- Syöpätauteihin, erityisesti adenokarsinoomiin, liittyy yleistynyt tukosalttius, ja idiopaattisen SLT/KE:n ilmaantuminen voi paljastaa syövän
- 5 %:lta idiopaattisen SLT/KE:n sairastaneista potilaista löydetään syöpä vuoden kuluessa
- Potilailla, joilla idiopaattinen tukos uusiutuu, osuus on 15 %
- Suurin tromboosiriski liittyy vatsalaukun ja haiman syöpiin
- Rutiininomaista laajaa syöpäseulontaa ei pidetä kustannustehokkaana, mutta tarkan kliinisen tutkimuksen mukaan ohjatut lisäselvitykset/kuvantamiset ovat perusteltuja
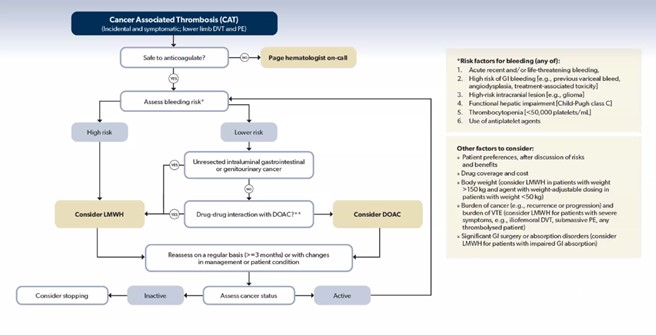
- Aiemmin syöpäpotilaiden SLT/KE:n hoitoon suositeltiin vain LMWH, mutta viime vuosina on tullut hyvää tutkimusnäyttöä myös suorista antikoagulanteista
- Varfariinia ei suositella syöpäpotilaille, paitsi mekaanisen tekoläpän yhteydessä, lisääntyneen vuotovaaran ja heikomman tukoksenesto tehon takia
- Syöpäpotilaan tukos/vuotoriski tulee arvioida ja suunnitella AK-hoito yksilöllisesti potilaan mielipidettä kuunnellen
- Syöpäpotilaan tukosprofylaksiaan sairaalahoidossa ja leikkausten yhteydessä tulee kiinnittää erityistä huomioita
LMWH hoidon periaatteet syöpätautiin liittyvässä SLT/KEssa
- Vaihtoehtoina ovat enoksapariini (Klexane/Inhixa), daltepariinilla (Fragmin), tintsapariini (Innohep)
- Ilmeisesti enoksapariniin biosimilaarit ovat teholtaan Klexane-valmistettava vastaavia, vaikka niistä ei ole suoraa tutkimusnäyttöä
- Jos hoito näyttää pitkittyvän yli 6kk trombiprofylaksiana, kannattaa aloittaa daltepariini tai tintsapariinin KELA korvattavuusmahdollisuuden takia
- Tukoksen hoitona on täysi hoitoannos 4-6 viikkoa, jonka jälkeen annosvähennys 25%
- 3-6kk käytön jälkeen siirrytään profylaksia-annokseen, tehostettuun profylaksia annokseen tai suoraan antikoagulanttiin Yli 5 vrk hoidossa tulee mitata anti-FXa erityisesti suuren vuotoriskin syöpäpotilailla
- ks. LMWH annokset tukosprofylaksiassa
LMWH hoitoannokset laskimotukoksessa. Vuotoriskin potilailla, kuten GI-kanavan syövissä tulee annosta pienentää. Munuaisten vajaatoimintapotilailla tulee enoksapariinin ja daltepariinin annoksia pienentää (25%-50%). Tintsapariinia voidaan käyttää ad eGFR 20ml/min tasolle saakka.
|
Enoksapariini (Klexane/Inhixa) |
1 mg/kg x 2 s.c. |
|
Daltepariini (Fragmin) |
100 ky/kg x 2 s.c. |
|
Tintsapariini (Innohep) |
175 KY/kg x 1 s.c.: < 60 kg 10 000KY 60-80kg 14 000KY > 80kg 18 000 KY
|
|
Huom. hoitotason määrittäminen anti-FXa-mittauksin: Tavoite: Anti-FXa 0.3 – 0.5 ennen seuraavaa pistosta |
|
LMWH korvattavuus syöpätauteihin liittyvässä tromboemboliassa ja sen estossa
- Inhixa, Enoxaparin Becat ja Ghemaxan-valmisteilla on 6kk Kela-korvaus reseptimerkinnällä
- Potilaille, joille on myönnetty erityiskorvausoikeus 115 (rintasyöpä), 116 (eturauhassyöpä), 117 (leukemiat, muut pahanlaatuiset veri- ja luuydintaudit sekä pahanlaatuiset imukudostaudit), 128 (gynekologiset syövät) tai 130 (pahanlaatuiset kasvaimet, joita ei ole edellä erikseen mainittu) ja
- jotka sairastavat aktiivista syöpätautia ja
- joiden laskimon tromboembolia on todettu syöpähoidon yhteydessä.
- lääkärin lääkemääräyksen kohtaan 'Perustelut' tekemällä merkinnällä '
- Tromboembolia
- Laskimotukos tai
- Keuhkoembolia,
- jonka jälkeen on merkitty tromboembolian toteamisen päivämäärä
- Tintsapariini ja daltepariini ovat korvattavia yli 6kk hoidossa syöpäpotilailla B-lausunnolla
- Faktori 10a estäjät ovat uuden tutkimustiedon valossa vaihtoehtoja LMWH:lle syöpään liittyvän tromboosin hoitoon. Paras tutkimusnäyttö on tällä hetkellä apiksabaanista:
- Apiksabaanista (Eliquis): apiksabaani vähensi trendinomaisesti SLT/KE riskiä 37% vrt. daltepariniin (p=0.09) ilman merkittävän verenvuotoriskin kasvua (Caravaggio tutkimus). Tutkimuksessa ei ollut leukemiapotilailta eikä potilaita, joilla oli kallonsisäinen kasvain.
- Edoksabaanista (Lixiana): edoksabaani vähensi trendinomaisesti 29%:lla SLT/KE riskiä verrattuna daltepariinin (p=0.09), mutta vuodot myös lisääntyivät tilastollisesti merkittävästi 1.8-kertaisesti (Hokusai-VTE tutkimus)
- Rivaroksabaanista (Xatelto) on tehty pienempi tutkimus (Select-D tutkimus), jonka perusteella se vähensi SLT/KE riskiä 57%, mutta lisäsi vuotovaaraa 3.8-kertaiseksi.
- Annokset ovat samoja kuin muissakin SLT/KE indikaatioissa
- 6kk Kela-korvattavuus reseptimerkinnällä
- Edoksabaania käytettäessä tulisi käyttää ensin 5 vrk LMWH yksinään, jonka jälkeen vaihdetaan edoksabaani
- Syöpäpotilaalta tulee seurata PVK ja krea 3kk välein
- Seuraavissa syöpätyypeissä on toistaiseksi suorien antikoagulanttien käyttöä ei suositella:
- Limakalvoille rajoittuneissa syövissä niitä ei kannata käyttää lisääntyneet vuotovaaran takia (GI-kanavan ja uroteliaalisyövät)
- Potilailla, joilla on kallonsisäinen tuumori/metastaaseja
- Leukemia
- Lääkeaineinteraktiot esim. sytostaattien kanssa on selvitettävä
- Edut vs. LMWH
- Suun kautta otettava valmiste on syöpäpotilaalle helpompi kuin LMWH
- Suora antikoagulantti on syöpäpotilaalle edullisempi kuin LMWH
- Vähemmän uusintatukoksia kuin LMWH:lla
- Apiksabaani ei lisännyt vuotovaaraa (tutkimuksesta oli poissuljettu leukemiapotilaat ja potilaat, joilla oli kallonsisäinen tuumori)
- ESMO 2011 / NICE 2018 / ITAC-CME 2019 / ISTH 2019 suositusten konsensus:
- Sairaalahoidossa olevallla syöpäpotilaalla tulee olla tukosprofylaksia (LMWH)
- Syöpäkirurgiassa ja syöpäpotilaan vatsan ja lantion alueen leikkausten yhteydessä tulee olla tukosprofylaksia, joka jatkuu 1kk leikkauksen jälkeen
- Ambulatorisilla sytostaattihoidoissa olevilla syöpäpotilailla ei suositella rutiinin omaista trombiprofylaksiaa, mutta voidaan yksilöllisesti harkita suuren vaaran (Khorana pisteet ≥2) potilailla
- Yhdistelmähoitoa saavilla myeloomapotilailla suositellaan trombiprofylaksiaa
- Solunsalpaajahoitoa saavilla haimasyöpäpotilailla, joilla on pieni vuotoriski, suositellaan trombiprofylaksiaa
- Jos potilas on jo sairastanut tukoksen, tulisi 6kk hoidon jälkeen jatkaa trombiprofylaksiaa seuraavilla potilailla (Thrombosis Canada):
- Sytostaattihoidossa olevat potilaat
- Metastaattinen syöpä
- Etenevä tai uusiutunut syöpä
- Muita riskitekijöitä tukokselle esim. keskuslaskimokatetri
- Apiksabaania (Eliquis) voi harkita trombiprolylaksiana syöpäpotilailla annoksella 2.5mg x 2 (AVERT-tutkimus): vähensi laskimotukoksia 59% vs. placebo 6kk aikana. Hoidon aikana ei ollut merkittäviä vuotoja merkittävästi enemmän kuin placebo-ryhmässä.
- B-lausunto vaaditaan Kela-korvattavuuden saamiseksi suorista antikoagulanteista 6kk hoidon jälkeiseen SLT/KE uusiutumisen estoon
Profylaktisen LMWH annostelu
|
LMWH |
Paino < 50 kg |
Paino 50–90 kg |
Paino > 90 kg |
Korotettu annos hyvin suuren riskin potilaille |
|
Enoksapariini |
20 mg x 1 |
40 mg x 1 |
60 mg x 1 |
40 mg x 2/ 80 mg x 1 |
|
Daltepariini |
2500 yks x 1 |
5000 yks x 1 |
7500 yks x 1 |
5000 yks x 2 / 10 000 IU x1 |
|
Tintsapariini |
3500 yks x 1 |
4500 yks x 1 |
7000 yks x 1 |
9000 yks x 1 |
|
Huom. ainakin suuren vuotovaaran potilaalla tavoitetason tarkistaminen anti-FXa-mittauksin: Tavoite: Anti-FXa 0.1– 0.3 ennen seuraavaa pistosta |
||||
CANCER AND THROMBOSIS. Thrombosis Canada 2020.
Agnelli G, et al. Apixaban for the treatment of venous thromboembolism associated with cancer. N Engl J Med 2020; 382(17):1599-1607.
Khorana AA, et al. Rivaroxaban for thromboprophylaxis in high-risk ambulatory patients with cancer. N Engl J Med 2019;380(8):720-728.
Key N, et al. Venous thromboembolism prophylaxis and treatment in patients with cancer: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol 2020;38(5):496-520.
Raskob G, et al. Edoxaban for the treatment of cancer-associated venous thromboembolism. N Engl J Med 2018;378:615-624.
Samuelson B, et al. Management of cancer-associated thrombosis in patients with thrombocytopenia: guidance from the SSC of the ISTH. J Thromb Haemost 2018;16:1-4.
Young AM, et al. Comparison of an oral factor Xa inhibitor with low molecular weight heparin in patients with cancer with venous thromboembolism: results of randomized trial (SELECT-D). J Clin Oncol 2018;36(20):2017-2023.